Что такое лучевая терапия? Словарь радиотерапевта
Елена Ивановна Тюряева, онколог и радиотерапевт НМИЦ онкологии им. Н.Н. Петрова, рассказала о возможностях современной лучевой терапии и ее значении в борьбе с онкологическими заболеваниями.
Когда появилась лучевая терапия?
В 1896 году в Вене доктор Фройнд впервые в мире применил рентгеновское излучение не для диагностики заболевания, а для лечения поверхностно расположенного доброкачественного образования. Несколькими годами позднее супруги Пьер и Мария Кюри открыли радиоактивный радий, который стал использоваться для контактной радионуклидной терапии.
За 125 лет лучевая терапия, проделав огромный путь совершенствования, получила широкое применение и вышла на качественно новый уровень. По мнению экспертного сообщества, в настоящее время не менее 60-70 % всех онкологических пациентов нуждается в лучевой терапии.
Что такое лучевая терапия?
Лучевая терапия – это процесс использования ионизирующего излучения для лечения различных заболеваний, прежде всего, онкологических. Это один из самых высокотехнологичных методов терапии, объединяющий инженерно-технические разработки, физико-математические модели и достижения информационных технологий. Лучевая терапия требует специалистов-радиотерапевтов знаний в области биологии, анатомии, радиобиологии, лучевой диагностики и общей онкологии.
Цели лучевой терапии
Задача лучевой терапии – достижение максимально возможного воздействия на опухоль и зоны ее клинического и субклинического распространения с высокой степенью точности и минимальными последствиями для окружающих тканей и органов. Цель лучевой терапии – разрушение опухолевой массы, в идеале приводящее к ее ликвидации или уменьшению размеров и метастатического потенциала, замедлению роста, что способствует продлению жизни и улучшению ее качества.
Лучевая терапия может использоваться на разных этапах лечения:
Предоперационная лучевая терапия
Задача предоперационной лучевой терапии — максимальное уменьшение объема опухоли, предотвращение попадания опухолевых клеток в лимфатическую или кровеносную систему, снижение риска развития отдаленных метастазов. При большинстве типов опухолей наиболее часто используется тандем лучевой и химиотерапии. Такое комбинированное воздействие позволяет в дальнейшем выполнить радикальное вмешательство с полным удалением новообразование. В ряде случаев предоперационная лучевая/химиолучевая терапия может приводить к полному регрессу опухоли, таким образом оказываясь самостоятельным методом лечения. Достижение полного клинического регресса, доказанное рентгенологическими методами (КТ, МРТ, ПЭТ-КТ) и подкрепленное данными биопсии, увеличивает возможность отсрочки или отказа от операции. Так, для опухолей прямой кишки, с полным клиническим ответом на химиолучевую терапию, получила признание концепция «waitandsee», т.е. «жди и наблюдай», закрепленная в международных и национальных стандартах лечения.
Интраоперационная лучевая терапия
Интраоперационная лучевая терапия – это облучение ложа опухоли сразу же после удаления ее хирургическим путем, непосредственно в операционном поле. Это действенный метод снижения риска развития местного рецидива. Интраоперационная лучевая терапия используется при опухолях молочной железы, при саркомах мягких тканей и даже при новообразованиях ЖКТ. Этот метод очень эффективен, но не лишен недостатков. Во-первых, для ее проведения необходимы специальные мобильные и компактные лучевые установки, которые могут располагаться в операционной. Во-вторых, однократная доза облучения может оказаться недостаточной, а объем интраоперационно облучаемых тканей достаточно ограничен. Интраоперационная лучевая терапия не позволяет воздействовать на пути лимфоотока. Трудно обеспечить точность дозиметрического планирования. Лучевая процедура увеличивает время пребывания пациента под наркозом и общую продолжительность вмешательства. Поэтому чаще интраоперационная лучевая терапия является составной частью сочетанного облучения, этапом комплексного лечения.
Послеоперационная лучевая терапия
Послеоперационная лучевая терапия – это воздействие на зону удаленной опухоли и пути лимфооттока для того, чтобы предотвратить возможность распространения отдельных опухолевых клеток в ходе хирургического вмешательства, т.е. снижения рисков развития местных и отдаленных метастазов. Послеоперационная лучевая терапия бывает необходима и после обширных операций, и после малоинвазивных вмешательств. В настоящее время наиболее часто применяется в лечении рака молочной железы, сарком мягких тканей, опухолей головы и шеи.
Самостоятельная или дефинитивная лучевая терапия
Самостоятельная лучевая/химиолучевая терапия показана в тех случаях, когда ее эффективность сравнима с радикальным оперативным лечением, т.е. при раннем раке, или, напротив, когда радикальное вмешательство невозможно – при наличии общих противопоказаний или из-за распространенности опухоли. В настоящее время рассматривается в качестве альтернативного метода лечения ранних опухолей голосового отдела гортани, ряда новообразований кожи. Наибольшее применение нашла в лечении рака предстательной железы. В сочетании с химиотерапией успешно используется при ранних опухолях пищевода, анального канала. Химиолучевое лечение является ведущим методом лечения рака шейки матки.
Наконец, лучевая терапия применяется для устранения симптомов опухолевого заболевания, таких, как боль, нарушение глотания и др. (симптоматическая лучевая терапия) или сдерживания опухолевого процесса (паллиативная лучевая терапия).
Технология лучевой терапии
Последовательность лечебных мероприятий для каждого больного принимается на онкологическом консилиуме в составе хирурга-онколога, химиотерапевта и радиотерапевта. Определив показания к лучевому лечению, врач-радиотерапевт формулирует общий план лечения: продолжительность курса, режим фракционирования дозы (доза за один сеанс облучения), суммарную дозу облучения, необходимость одновременного химиолучевого лечения, применения радиомодификаторов. Проведению сеансов облучения предшествуетэтап предлучевой подготовки.
Предлучевая подготовка включает:
Компьютерная топометрия
Создание индивидуальной дозиметрической карты облучения начинается с компьютерной топометрии, которую проводит врач-рентгенолог совместно с радиотерапевтом. На компьютерном томографе-симуляторе, с теми же фиксирующими приспособления и в том же положении, в котором будет проводиться лечение, сканируется область анатомического расположения опухоли (грудная клетка, брюшная полость, головной мозг и т.д.). Оцениваются структурные и анатомические особенности — локализация опухоли, протяженность объема, взаимоотношение со смежными органами, плотность внутренних тканей. Во время этой процедуры на кожу больного выносятся графические ориентиры –метки для центрации пучков излучения, которые в дальнейшем позволят ускорить навигацию в процессе проведения сеансов лечения. Последовательность компьютерных сканов передается на планирующую станцию для создания индивидуального плана облучения.
Контуринг мишени и смежных органов
Дальше наступает этап обработки полученных изображений. Сканы импортируются в планирующую систему, где врач-радиотерапевт с помощью врача-рентгенолога производит выделение очертаний (оконтуривание) опухолевой мишени, всех смежных органов в каждом полученном скане. На основании совокупности объемных изображений в дальнейшем производится расчет дозных нагрузок в ходе лечения на опухоль и соседние органы с учетом их толерантности к облучению.
Дозиметрическое планирование
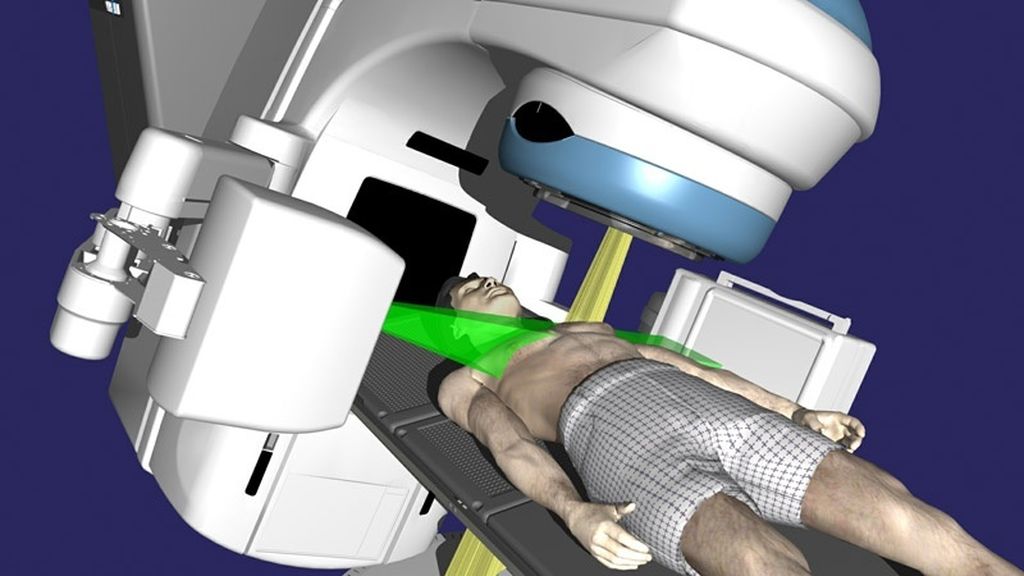
После завершения оконтуривания, оценки расположения опухоли и смежных органов, наступает этап дозиметрического планированиякурса лучевого лечения, который выполняется медицинскими физиками.Дозиметрическое планирование – это подбор количества и условий формирования пучков излучения, их пространственного размещения для того, чтобы подвести к опухоли максимально возможную терапевтическую дозу с минимальными последствиями для соседних органов. Современные медицинские ускорители, обладающие многолепестковыми коллиматорами, позволяют формировать поля сложной конфигурации, максимально точно соответствующие объему и форме облучаемой мишени, производя т.н. конформное облучение. Исходя из поставленных задач, оптимальный охват мишени может быть спланирован с использованием 3D многопольного облучения с объемно-модулируемой интенсивностью (IMRT) или дуговой модулируемой интенсивностью пучка излучения (VMAT).
На изображении представлен пример 3D многопольного излучения. Видно, что для облучения опухоли используется 3 пучка.
Средства иммобилизации пациента
Для того, чтобы осуществлять точную подачу ионизирующего излучения к облучаемой мишени, необходимо четко воспроизводить то положение, в котором шел процессе подготовки к лучевому лечению, т.е. компьютерная топометрия и дозиметрическое планирование. Это обеспечивается разнообразными средствами для укладки, иммобилизации пациента. Они могут быть в виде разных штатных дек с подголовниками, креплениями, валикамии подставками для рук, ног, таза. Есть и индивидуальные средства. Например, вакуумные матрасы и термопластические маски, фиксирующие индивидуальные формы тела пациента в положении облучения. Эти приспособления позволяют избегать смещения облучаемой зоны из-за непроизвольных движений пациента.
Виды лучевой терапии
Дистанционная лучевая терапия
При дистанционном облучении источник ионизирующего излучения находится на расстоянии — вне тела пациента и вне опухолевой мишени. В зависимости от типа излучающего аппарата дистанционная лучевая терапия включает в себя рентгенотерапию, телегамматерапию, электронную и протонную терапию. Наиболее распространенным вариантом дистанционной лучевой терапии в настоящее время является облучение высокоэнергетическими фотонами и пучками электронов на медицинских ускорителях электронов. Современные модели ускорителей с помощью компьютерного управления параметрами и геометрией пучка излучения обеспечивают максимальное соответствие формы очага-мишени и распределения в нем дозы облучения. Возможность формирования пучков тормозного (фотонного) и корпускулярного (электронного) излучения с различной мощностью — от 6 МэВ до 18-20 МэВ — позволяет облучать как поверхностные, так и расположенные глубоко в тканях тела объекты.
Особое внимание в настоящее время приковано к протонной терапии. Первый в России клинический центр протонной терапии был построен в Санкт-Петербурге. Преимущество метода состоит в особенности тяжелых заряженных частиц (протонов). Протоны максимально высвобождают энергию торможения в конце пути своего пробега, причем спад дозы от 90% до 20% происходит на дистанции 2-5 мм. Такая возможность концентрации дозы в конце пробега частицы позволяет не только наилучшим образом сконцентрировать дозу, но и минимизировать лучевую нагрузку на ткани по ходу пучка и за патологическим очагом. Протонная терапия актуальна в онкоофтальмологии, радионейрохирургии, и особенно для пациентов детского возраста. В настоящее время сфера применения протонной терапии расширяется, однако пока использование метода существенно ограничивается его высокой стоимостью.
Современной технологией дистанционного облучения является стереотаксическая лучевая терапия – метод высокопрецизионного крупнофракционного облучения опухолей размером не более 5 см. В отличие от радиохирургии, разработанной для лечения опухолей головного мозга, использующей однократное облучение, общее число фракций при стереотаксическом облучении варьирует от 1 до 5-6. Разовая очаговая доза составляет от 8 Гр до 20 Гр, суммарная эквивалентная поглощенная доза от 50 Гр до 150 Гр, что существенно выше, чем при классическом варианте фракционирования лучевой терапии. Гамма-нож — один из видов лучевых установок для стереотаксического облучения новообразований головного мозга. Ускорители с микролепестковыми коллиматорами позволяют производить стереотаксическое облучение любых очагов (головной мозг, предстательная железа, легкое, кости, печень, поджелудочная железа, лимфоузлы, мягкие ткани). При стереотаксическом облучении обязательно учитываются смещения очага, возникающие при дыхании. Для этого запись КТ-изображений при КТ-симуляции производится с синхронизацией дыхательного цикла (4D лучевая терапия).
Контактная лучевая терапия
При контактной лучевой терапии или брахитерапии, источник излучения вводится внутрь пораженного органа. Преимущества такого вида терапии – это короткий курс, высокая точность и низкая нагрузка на смежные органы, что очень важно для дальнейшего качества жизни пациентов. Для брахитерапии используются различные радиоактивные источники – изотопы кобальта (Co⁶⁰), иридия (Ir¹⁹²), цезия (Cs¹³⁶).
Контактная лучевая терапия имеет разновидности: аппликационная, внутриполостная, внутритканевая и радионуклиднаялучевая терапия.
Аппликационная лучевая терапия
При аппликационной лучевой терапии источник располагается на поверхности облучаемого наружного объекта (кожа).
Внутриполостная лучевая терапия
При внутриполостной лучевой терапии источник подводят напрямую к опухоли в полости органа. Наиболее часто применяется при раке прямой кишки, анального канала, пищевода, при внутрибронхиальных образованиях. Внутриполостная или внутрипросветная брахитерапия чаще используется как этап сочетанной лучевой терапии, до или после дистанционного облучения. Однако нередко брахитерапия как самостоятельный метод достаточна после малоинвазивных операций при ранних стадиях рака. При паллиативном лечении рака пищевода брахитерапия — эффективный способ устранения дисфагии (расстройства акта глотания).
Внутритканевая лучевая терапия
При внутритканевой лучевой терапии источник вводят в ткани самой опухоли. Внутритканевая брахитерапия наиболее распространена при опухолях предстательной железы, широко используется при облучении молочной железы, при опухолях головы и шеи и при новообразованиях в печени.
Радионуклидная лучевая терапия
Перспективы лучевой терапии
Основными векторами дальнейшего развития лучевой терапии являются усовершенствование методик визуально ориентированного подведения дозы, влияние на радиочувствительность опухолевых клеток с помощью радиомодификаторов, применений комбинаций лучевого лечения с новыми химио- и иммунотерапевтическими агентами.
Беседовала
Анастасия Башкова
практикант отдела по связям с общественностью НМИЦ онкологии им. Н. Н. Петрова
Санкт-Петербургский государственный университет
Высшая школа журналистики и массовых коммуникаций
Одновременная химиолучевая терапия
Определение понятия
Теоретические основы
Из клинических и экспериментальных исследований можно определить следующие преимущества одновременной химиолучевой терапии по сравнению с однократной лучевой терапией или химиотерапией или последовательной комбинацией обоих методов (таблица 1):
Исходя из этих соображений, можно выделит конкретные условия, при которых одновременная химиолучеваятерапия (ХЛТ) кроме лечебной цели имеет еще и теоретическую целесообразность:
Радиобиологические эффекты одновременной химиолучевой терапии
Эффект
Радиационно-биологическое обоснование
Клиническое значение
Аддитивный противоопухолевый эффект
Больший цитотоксический эффект за счет добавления отдельных эффектов лучевой терапии и химиотерапии
Различные точки атаки
Химиотерапия убивает радиорезистентные клетки и наоборот
Химиотерапия может повышать интенсивность внутриклеточного облучения, в частности, например, в гипоксических клетках
Побочные эффекты распространяются на разные системы органов, следует избегать токсических доз соответствующих методов лечения
Интенсификация благодаря более короткому общему времени лечения по сравнению с последовательным проведением химиолучевой терапии
Влияет на пролиферацию опухоли (репопуляцию) во время нескольких недель лучевой- или химиолучевой терапии
Протоколы лечения для одновременной химиолучевой терапии
Основой протоколов клинического лечения обычно является режим лучевой терапии с дозой облучения в диапазоне от 50 до 60 Грей. Следует избегать соответствующего снижения дозы облучения, поскольку химиотерапия не может заменить лучевую терапию. Одновременно с лучевой терапией выполняются инъекции одного или двух цитостатических средств, которые являются наиболее эффективными в соответствующей опухолевой структуре, их вводят в эффективной дозировке, которая также является обычной в случае проведения только химиотерапии. В течение нескольких недель лучевой терапии обычно могут быть проведены два или три курса химиотерапии. При этом выбор наименования и дозировки цитостатиков проходит таким образом, что нет необходимости достигать соответствующих компромиссов в лучевой терапии, являющейся основным терапевтическим элементом.
Клинические результаты и текущий спектр показаний
Превосходство одновременной химиолучевой терапии с применением Цисплатина / 5-фторурацила по сравнению с применением только лучевой терапии при локально прогрессирующих плоскоклеточных карциномах в области головы и шеи
Только лучевая терапия
Одновременная химиолучевая терапия
Клиническая значимость
Локальный контроль опухоли через три года
p Трехлетняя выживаемость
p Результаты рандомизированного исследования отдела радиационной онкологии Немецкого общества борьбы с раковыми заболеваниями (Вендт и др., 1997)
Побочные эффекты и поддерживающая терапия
Согласно имеющимся в настоящее время клиническим данным, по крайней мере, при установленных показаниях (таблица 3) повышенный риск поздних эффектов отсутствует, тем не менее, в данной связи необходимы дальнейшие долгосрочные наблюдения.
Показания к одновременной химиолучевой терапии (ХЛТ), согласно действующим рекомендациям Немецкого общества борьбы с раковыми заболеваниями
Вид опухоли/стадия
Эффект одновременной ХЛТ
Дополнительные методы лечения
Доза облучения
(Гр) /цитостатики
Анальные карциномы, все стадии (плоскоклеточная карцинома, базалоидная карцинома)
Выживаемость, как при радикальном хирургическом лечении, сохранение сфинктера примерно у 80%
Удаление прямой кишки при наличии остаточной опухоли или при рецидиве
около 50Гр / Митомицин С + 5-фторурацил
Прогрессирующие плоскоклеточные карциномы в полости рта и в горле (T3-4 или N3)
Лучшая выживаемость, чем при проведении только лучевой терапии, сохранение органов более чем в 90% случаев
В отдельных случаях операция по поводу остаточной опухоли или рецидива
60-70 Гр / Цисплатин + 5-фторурацил
Локально прогрессирующие карциномы прямой кишки (T4)
Предоперационно для уменьшения размеров опухоли для последующего куративного хирургического лечения
В основном резекция / экстирпация прямой кишки после химиолучевой терапии
Локально прогрессирующие карциномы прямой кишки pT3-4 или pN1-3 после куративного хирургического лечения
Улучшение выживаемости и более оптимальный локальный контроль опухоли с помощью послеоперационной ХЛТ
Дополнительная химиотерапия с 5-фторурацилом до / после ХЛТ
Неоперабельные карциномы мочевого пузыря T3-T4
Выживаемость как при радикальной операции, сохранение мочевого пузыря примерно в 70% случаев
Необходима радикальная цистэктомия при наличии остаточной опухоли или при рецидиве
54-60 Гр / Цисплатин
Неоперабельные карциномы поджелудочной железы
Наиболее эффективная терапия при неоперабельности
Выводы
В целом, результаты клинических исследований, проведенных до настоящего времени, показывают, что при некоторых онкологических заболеваниях оптимальная комбинация лучевой терапии и химиотерапии может обеспечить успешный исход терапии.
Химиотерапия: что это и как ее делают при онкологии
Лекарственная противоопухолевая терапия, в том числе и химиотерапия, – один из основных методов лечения рака. При химиотерапии в человеческий организм вводятся различные токсические вещества, которые губительно воздействуют на клетки злокачественных опухолей. Важно при этом, чтобы яды и токсины оказывали наименьшее отрицательное воздействие на весь организм больного.
Схемы химиотерапевтического лечения регламентируются международными методиками и правилами, и рассчитываются индивидуально. Врач-химиотерапевт подбирает пациенту лечение, руководствуясь различными критериями, среди которых:
Виды химиотерапии
Сложные комбинации из нескольких химиопрепаратов на сегодняшний день используются чаще, так как они более эффективные.
Химиотерапия нередко применяется как часть комбинированного лечения рака:
Дозы и режимы применения противоопухолевых препаратов
Противоопухолевые лекарственные препараты и их дозировка подбираются строго индивидуально.
У каждого препарата имеются свои характеристики и особенности. При проведении химиотерапии важными являются следующие параметры:
Дозу препарата рассчитывают исходя из схемы химиотерапии, роста, веса, возраста, состояния больного, а в некоторых случаях, на основании лабораторных показателей пациента.
Режимы
Если необходимо повысить интенсивность химиотерапии, то увеличивают дозу препарата, это так называемая высокодозная терапия, либо сокращают интервал между курсами ХТ, то есть вводят уплотненные режимы.
Также существуют метрономные режимы применения цитостатических препаратов, когда вводятся малые дозы препаратов, но постоянно в течение длительного времени.
После каждого курса химитерапевтического лечения обязательно делается определенный перерыв для восстановления организма. Как правило, повторные курсы ХТ проводят через каждые три-четыре недели, это период, в течение которого восстанавливаются показатели лейкоцитов, тромбоцитов и пр.
При использовании некоторых химиопрепаратов, к примеру, нитрозопроизводных, этот интервал увеличивается до 6 недель.
Продолжительность лечения и количество курсов химиотерапии зависит от вида опухоли, от особенностей течения болезни от того, как организм реагирует на лечение. Иногда возникает необходимость прекратить или изменить лечение, и это решение принимает лечащий врач.
Способы применения химиопрепаратов
Правила введения противоопухолевых препаратов
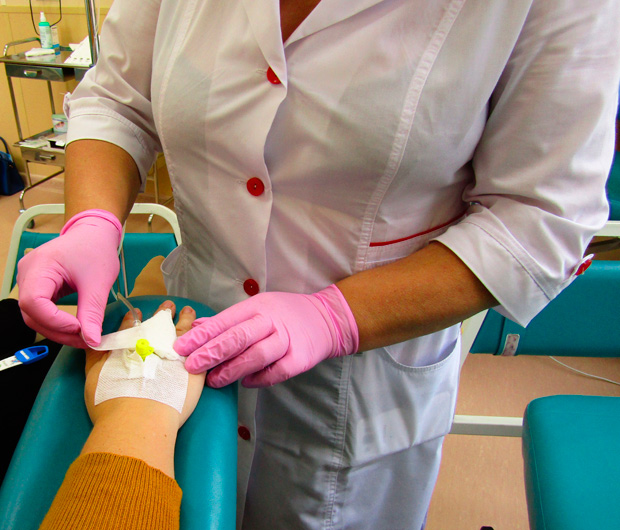
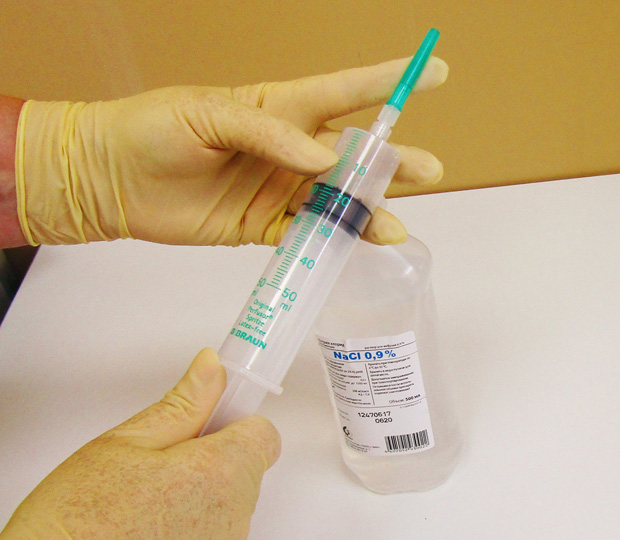
Наиболее широко используется внутривенное введение противоопухолевых средств. При этом врач обязательно учитывает индивидуальные особенности вен пациентов.
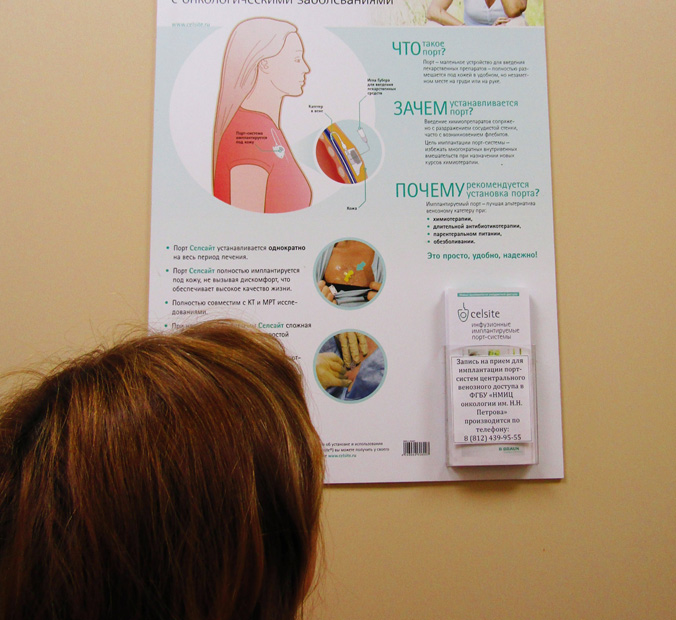
Имплантируемые порт-системы
Имплантируемая порт-система — это катетер, установленный в сосуд или полость и соединенный с ним резервуар-камера. Система «порт — катетер» широко используется в медицине уже более чем 30 лет.
Порт-системы помогают проходить лечение более эффективно, безопасно и качественно. Особенно актуальна их установка в качестве устройства сосудистого доступа пациентам, которым назначено длительное лечение, при осложнениях на фоне химиотерапии, которые привели к затруднению венозного доступа.
При этом терапию пациент может получать как в условиях стационара, так и амбулаторно.
Инфузия лекарственных препаратов производится с помощью специальных игл типа Губера, которые, пунктируя силиконовую мембрану порта, позволяют вводить инфузионный раствор в резервуар, не повреждая силиконовую мембрану. Далее препарат попадает через катетер в кровоток или полость, в зависимости от вида порт-системы и места расположения катетера.
Порт- система полностью скрыта под кожей. Поэтому она подходит для длительного использования, не обременяет пациента и не мешает проведению гигиенических процедур. Необходимо помнить, что при отсутствии использования порт-систему необходимо промывать как минимум 1 раз в 2 месяца.
Подготовка к химиотерапии
Чтобы не было проблем с поиском вен и установкой катетера за день до химиотерапии желательно выпить 1,5-2 литра жидкости.
Для тренировки вен рекомендуется периодически сжимать кистевой эспандер по 10 мин 3 раза в день или до усталости. При этом рука должна быть свешена ниже уровня сердца.
В день проведения ХТ нужно держать руки в тепле, возможно применение теплых обертываний на места инъекций. Можно периодически обрабатывать руки теплыми полотенцами.
Во время прохождения химиотерапии
В день химиотерапии, с утра необходимо позавтракать.
Далее необходимо соблюдать несколько несложных правил:
Об осложнениях после химиотерапии читайте здесь.
Возможно ли повысить эффективность химиотерапии?
Поиск основных направлений повышения эффективности терапии опухолей осуществляется в разных направлениях: